DIAGRAMA HIERRO-CARBONO
Es un tipo de diagrama donde se representan las transformaciones que sufren los aceros al
carbono con la temperatura adecuada, considerando que el calentamiento o enfriamiento de
la mezcla se realiza muy lentamente, de modo tal que los procesos de homogenización tengan tiempo para completarse. Dicho diagrama se obtiene
experimentalmente identificando los puntos críticos —temperaturas a las que se
producen las sucesivas transformaciones— por diversos métodos.
En este caso, la descripción que se hará sobre este diagrama va enfocada enfocada hasta un 6,67% en peso de carbono.
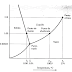
Figura #1: Diagrama de fases Hierro-Carburo de hierro hasta 6,67% Peso de Carbono
Es importante acotar antes de iniciar el desglose, que este diagrama de fases no es un diagrama de equilibrio verdadero, ya que el compuesto Carburo de Hierro (Fe3C) que se ha formado, no es una verdadera fase de equilibrio. Bajo ciertas condiciones y características, el Fe3C, que se le denomina cementita puede descomponerse en las fases mas estables de hierro y carbono, como grafito. No obstante, en la mayor parte de las condiciones practicas, el Fe3C es muy estable, y por ende, es tratado como una fase de equilibrios.
CARACTERÍSTICAS DEL DIAGRAMA Fe-Fe3C
Este contiene las siguientes fases solidas:
- Ferrita (α): Esta fase es una disolución solida intersticial de carbono en la red cristalina del hierro BCC. Como se indica en el diagrama de fases Fe-FeC3, el carbono solo es soluble en Ferrita (α), por lo que alcanza una solubilidad máxima en estado solido del 0,02% a 723 *C. La solubilidad del carbono en la Ferrita (α) disminuye a un 0,005% a 0 *C.
- Austenita (γ): La disolución solida intersticial de Carbono en Hierro γ se denomina austenita. La austenita tiene una red cristalina FCC y mucha mayor solubilidad en estado solido para el carbono que la Ferrita (α). La máxima solubilidad en estado solido del carbono en la austenita es del 2,08% a 1148 *C y disminuye a un 0,8% *C a 723*.
- Cementita (Fe3C): Tiene unos limites de solubilidad despreciables y una composición de un 6,67 % de Carbono y un 93,3% de Hierro. La cementita es un compuesto duro y frágil.
- Ferrita (δ): La disolución solida intersticial de Carbono en Hierro δ se llama Ferrita (δ). Tiene una estructura cristalina BCC como la Ferrita (α) pero con una constante de celda mayor. La máxima solubilidad del Carbono en estado solido en la Ferrita (δ) es de 0,09% a 1465 *C.
- Reacción Peritectica: En este punto, un liquido del 0,53% de Carbono se denomina Ferrita (δ) de un 0,09% de C para formar Austenita (γ) 0,17% de Carbono. Tiene lugar a 1495 *C.
Liquido (0,53% C) + δ (0,09 % C) 1495 *C> γ (0,17% C)
- Reacción Eutectica: En el punto de reacción, el liquido 4,3% de C en forma de Austenita (γ) del 2,08% C y el compuesto intermetalico Fe3C, que contiene 6,67% de C. Esta reacción tiene lugar a 1148 *C.
Liquido (4,3% C) 1148 *C> γ (2,08% C) + Fe3C (6,67% C)
- Reacción Eutectoide: En este punto de reacción, la austenita solida de un 0,8% C da lugar a Ferrita (α) con un 0,02% de C y Fe3C que tiene un 6,67% de C, reaccion que tiene lugar a 723 *C.
Austenita (γ) (0,8% C) 723 *C> Ferrita (α) (0,02% C) + Fe3C (6,67% C)
Esta reacción eutectoide, que tiene lugar totalmente en estado solido, es importante para algunos tratamientos térmicos de los aceros ordinarios. Un acero al carbono que contiene un 0,8% de C se llama acero eutectoide, puesto que cuanto la austenita de esta composición se enfría lentamente por debajo de la temperatura eutectoide se forma una estructura totalmente eutectoide de Ferrita (α) y Fe3C. Si un acero al carbono contiene menos de 0,8% de C se llama Hipoeutectoide, y si tiene mas se denomina hipereutectoide.











Solo se ve esta publicación.
ResponderEliminar