RESUMEN
TRACCIÓN
Con la presente publicación se buscara puntualizar elementos claves de las practicas realizadas en el laboratorio. Los informes para estas experiencias de Dureza, Tracción e Impacto han dejado resultados prácticos que se pueden constatar con los fundamentos básicos vistos en la materia de Ciencias de los materiales. Es importante acotar que los objetivos en os casos planteados fueron logrados satisfactoriamente dejando aspectos importante para el respectivo análisis postlaboratorio.
El objetivo de esta experiencia era determinar las propiedades mecánicas de un material, aplicando un Ensayo de Tracción, realizando la gestión adecuada de los desechos generados.
Un Ensayo de Tracción es el ensayo mediante el cual se obtiene información básica sobre las propiedades mecánicas de los materiales metálicos, por ende es un ensayo mecánico de tipo destructivo. Consiste en someter una probeta a una fuerza de tensión axial mientras se van midiendo simultáneamente los correspondientes alargamientos de la misma hasta producirse la rotura del material. Se utiliza una máquina de tracción que consta de dos mordazas, una fija y otra móvil, donde se coloca la probeta a estudiar y se mide la carga mientras se aplica el desplazamiento de la mordaza móvil.
La realización de este ensayo permite afianzar los conocimientos, que en la cátedra de Tecnología de los Materiales y Manufactura son suministrados; además es un ensayo importante a nivel industrial, porque mediante este se determinan las propiedades mecánicas del material así como también su posterior uso o aplicación.
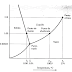
Durante la tracción de la probeta, la deformación se concentra en la región central más estrecha, la cual tiene una sección transversal uniforme. La muestra se sostiene por sus extremos en la máquina por medio de soportes o mordazas que a su vez someten la muestra a tensión a una velocidad constante. La máquina al mismo tiempo mide la carga aplicada instantáneamente y la elongación resultante, al igual que permite obtener una curva de Esfuerzo vs %Elongación, así como también Fuerza vs Elongación, etc., que servirán para realizar los cálculos y análisis correspondiente a este ensayo.
Palabras claves:
- Longitud calibrada (L): Es la distancia entre dos puntos marcados sobre la probeta, en relación a la cual se calculará el alargamiento de rotura.
- Punto de Fluencia: Es el esfuerzo para el cual un material se sigue deformando sin incremento en la carga aplicada.
- Límite Elástico: Es el esfuerzo máximo, que al dejar de actuar no produce deformaciones permanentes en el material. Se usa en aquellos materiales cuyo punto de fluencia en la curva Esfuerzo vs Deformación no está bien definido.
- Resistencia a la Tracción (σT): Es el valor del esfuerzo correspondiente al valor máximo de carga aplicada que obtiene durante el ensayo.
- Punto de Rotura: Es el punto en el cual la probeta se fractura al aplicar una carga. Tenacidad: Es la energía que puede absorber una probeta antes de producirse la rotura.
- Ductilidad: Es la propiedad de un material a deformarse plásticamente antes de la rotura.
- Deformación de rotura (ε): Es la relación entre el incremento de la longitud calibrada (ΔLO) de la probeta luego de ser sometida a la aplicación de una carga hasta el momento de rotura y la longitud original de la zona calibrada, expresada en porcentaje.
- Área de Estricción (q): Es la relación existente entre la disminución del área de la sección transversal de la probeta después de la rotura y el área de la sección transversal antes del ensayo, expresada en porcentaje.
- Sección Calibrada: Es el trozo de menor sección uniforme de la probeta de ensayo de tracción.
- Sección de Agarre: Es la zona de la probeta sobre la cual la mordaza de la máquina de ensayo realiza la sujeción.
- Fragilidad: Se define como la capacidad de un material de fracturarse con escasa deformación, a diferencia de los materiales dúctiles que se rompen tras sufrir acusadas deformaciones plásticas.
IMPACTO
El objetivo principal de esta experiencia consistía en evaluar la tenacidad de un material a diferentes temperaturas al estar sometido a un impacto, utilizando el Péndulo Charpy.
El Ensayo de Impacto Charpy consiste en romper de un sólo golpe con un péndulo normalizado, una probeta entallada en el centro y simplemente apoyada en sus extremos, por lo tanto, es un ensayo mecánico destructivo que permite calcular la resistencia de un material frente a situaciones de trabajo como el impacto. Este ensayo proporciona los datos necesarios para conocer cuanta energía logra disipar una probeta al ser golpeada por un péndulo en caída libre. Se utiliza una máquina llamada Péndulo de Charpy, la cual está construida e instalada en forma tal, que permanezca rígida y estable, evitando pérdidas de energía (por rotación o vibración), durante el ensayo. Consta de un martillo sujeto (desde su extremo superior) a un soporte de pie rígido que lleva un tablero de escala analógico, mientras que su extremo inferior queda libre simulando así un péndulo. Este ensayo es importante a nivel industrial, porque mediante él se determina qué tan dúctil o frágil es el material estudiado así como también su posterior uso o aplicación.
Durante el ensayo, un péndulo pesado (que inicia su movimiento desde una altura inicial) describirá un arco para luego golpear a una probeta desde el lado opuesto al entalle de la misma, por la cual se fracturará o se doblará en forma de U. Con el único fin de facilitar el inicio de una fisura (justo en el instante del impacto) la probeta posee un entalle estándar, a este entalle se le conoce como V – Notch.
La cantidad de energía absorbida por un material, al aplicarle un ensayo, está bajo la influencia de la temperatura y de la composición química; a la temperatura mencionada se le conoce como la Temperatura de Transición. La Temperatura de Transición es aquella a la cual un material cambia de un comportamiento dúctil a un comportamiento frágil y se puede definir como la energía promedio entre las regiones dúctil y frágil, a una energía absorbida específica, o al tener ciertas características en la fractura. No todos los materiales tienen una temperatura de transición bien definida. Los valores de energía disminuyen gradualmente e incluso a veces se incrementa conforme se reduce la temperatura. Existe otro tipo de Ensayo de Impacto, que generalmente se utiliza para materiales no metálicos, donde se utiliza un Péndulo Izod, ambas maquinarias (Péndulo Charpy y Péndulo Izod) tienen la misma finalidad que es calcular la resistencia que opone un material al ser sometido a fuerzas de impacto. La diferencia fundamental entre ellos es la colocación de la probeta; en el Ensayo Charpy es horizontal simplemente apoyada en sus extremos, mientras que en la Izod es vertical en voladizo empotrada en un extremo.
Palabras Claves:
- Tenacidad: Es la energía que puede absorber una probeta antes de producirse la rotura.
- Centro de Impacto: Es el punto donde el péndulo hace el impacto.
- Energía de Impacto: Es la energía cinética que lleva el péndulo en el momento del impacto.
- Energía Absorbida Charpy: Es la energía requerida (kgm) para romper la probeta, usando una máquina de impacto Charpy.
- Valor de Impacto Charpy: Es el valor obtenido (kgm/cm2) al dividir la energía absorbida Charpy (kgm) entre el área de la sección original (cm2) de la porción entallada.
- Energía Absorbida Izod: Es la energía (kgm) requerida para romper la probeta, haciendo uso de la máquina de impacto Izod.
- Valor de Impacto Izod: Es el valor obtenido (kgm/cm2) al dividir la energía absorbida Izod (kgm) entre el área de la sección original (cm2) de la porción entallada.
- Ductilidad: Es la propiedad de un material a deformarse plásticamente antes de la rotura.
- Fragilidad: Se define como la capacidad de un material de fracturarse con escasa deformación, a diferencia de los materiales dúctiles que se rompen tras sufrir acusadas deformaciones plásticas. Por lo tanto, si el material es dúctil es tenaz; si el material es frágil no es tenaz; el frágil disipa poca energía mientras que el dúctil disipa mucha.
DUREZA
El enfoque principal de esta practica de laboratorio era realizar ensayos de Dureza Rockwell sobre una muestra metálica.
El ensayo de Dureza Rockwell es un método para determinar la dureza, es decir, la resistencia de un material a ser penetrado. Para este ensayo se emplea un equipo llamado Durómetro; también se pueden utilizar diferentes escalas, las cuales provienen de la utilización de distintas combinaciones de penetradores y cargas, lo que permite ensayar prácticamente cualquier metal o aleación. Existen escalas de Dureza Rockwell y escalas de Dureza Rockwell Superficial. Toda muestra para Dureza Rockwell deberá estar preparada adecuadamente con el fin de que los resultados no se vean afectados por condiciones de una mala preparación. El ensayo de dureza es uno de los más utilizados y útiles en el campo de la metalurgia, mediante el se pueden predecir características y propiedades de los metales como no se podría hacer con un ningún otro ensayo.
Principio del Ensayo Rockwell: El ensayo consiste en imprimir en una probeta de características preestablecidas una huella usando un penetrador de tipo estandarizado (esfera de acero endurecido para Rockwell B y cono de diamante para A y C), en dos operaciones (precarga y carga) y medir el incremento de penetración “e” de la profundidad de la huella en las condiciones especificadas para el ensayo.
Principio del Ensayo Rockwell Superficial: El ensayo consiste en imprimir en una probeta de características preestablecidas una huella usando un penetrador de tipo estandarizado (esfera de acero endurecido para Rockwell Superficial T y cono de diamante para Rockwell Superficial N), en dos operaciones (precarga y carga) y medir el incremento de penetración “e” de la profundidad de la huella en las condiciones especificadas para el ensayo.
Penetradores o Indentadores: Hay dos tipos de penetradores o indentadores: unas bolas esféricas de acero endurecido (templado y pulido) y un penetrador cónico de diamante de vértice redondeado formando un casquete esférico, el cual se utiliza para los materiales más duros.
Penetrador esférico (Escala B y Escala Superficial T): En general, el penetrador esférico consiste de una bola acero templado y pulido, diámetro de 1,588 mm. Puede utilizarse una bola de otro material más duro, como por ejemplo carburo de tungsteno, en cuyo caso debe especificarse el material utilizado en el informe del ensayo, por cuanto la utilización de tales materiales dará resultados valores menores de dureza que los obtenidos con los penetradores de acero. La bola utilizada como penetrador debe poseer una dureza Vickers de 850 HV10 (tomando en cuenta la curvatura de la bola). La bola no debe poseer defectos superficiales.
Penetrador cónico (Escala A, Escala C y Escala Superficial N): Consiste en un cono de diamante, circular, recto, de punta redondeada con un ángulo interno de 120°. El penetrador debe estar exento de grietas y otros defectos superficiales.
Aspecto superficial de los penetradores: El aspecto superficial de los penetradores debe ser controlado con frecuencia, deben estar pulidos y exentos de grietas o de otro defecto superficial. Todo penetrador que presente, después del ensayo, una deformación tal que sobrepase la tolerancia, debe ser eliminado y descartados los resultados correspondientes.
Indicador de profundidad para Rockwell: El indicador de profundidad deber tener una tolerancia de ± 0,5 unidades de medida, es decir ± 0,001 mm. Indicador de profundidad para Rockwell Superficial El indicador de profundidad deber tener una tolerancia de ± 0,5 unidades de medida, es decir ± 0,0005 mm.
Soportes: El tipo de soporte a usar dependerá de la superficie a ser ensayada. Para el caso del ensayo de piezas cilíndricas se usa los soportes del tipo I y II. Para el caso del ensayo de piezas planas, se usa un soporte del tipo III. Para el caso del ensayo de piezas cóncavas con un diámetro de curva grande, se usa un soporte del tipo IV.
Método Rockwell (Escala A, B y C): Las escalas A y C deben aplicarse únicamente al ensayo de dureza de materiales superiores a 20 HRA y HRC. La escala B debe aplicarse al ensayo de dureza de materiales inferiores a 100 HRB. Ejemplo: Si el material es duro se utiliza la escala A (con indentador de cono de diamante y carga 60 Kgf) o la escala C (con indentador de cono diamante de cono de diamante y 150 Kgf). En caso contrario (materiales blandos), se utiliza la escala B con indentador de esfera 1/16 pulg y carga de 100 Kgf.
Método Rockwell Superficial (Escalas N y T): La escala N es usada en materiales similares a los ensayados en las escalas A y C, pero de no menor espesor o en aquellos casos en que se requiere una huella diminuta. La escala T es usada en materiales similares a los ensayados en la escala B, pero de menor espesor o en aquellos casos en que se requiera una huella diminuta.
Existen también otros tipos de ensayo de dureza, como por ejemplo el Ensayo Vickers y el Ensayo Brinell; en ambos ensayos se mide el tamaño de la huella, en Vickers la huella (diagonales de huella) dejada por el indentador es una pirámide de diamante de base cuadrada y para Brinell la huella (diámetro de huella) es una esfera de acero endurecido.